新聞中心
News Center
艾貝格司亭α全球III期注冊(cè)研究之GC-627-04研究數(shù)據(jù)公布
發(fā)布時(shí)間:2023-12-19
艾貝格司亭α(億立舒®)是一種新型長(zhǎng)效粒細(xì)胞集落刺激因子(G-CSF),是全球首個(gè)第三代長(zhǎng)效G-CSF創(chuàng)新藥。此前,中國(guó)生物制藥與億一生物簽訂商業(yè)化合作協(xié)議,獲得億立舒在中國(guó)境內(nèi)的所有知識(shí)產(chǎn)權(quán)和獨(dú)家商業(yè)化權(quán)益。2023年5月9日,艾貝格司亭α成功獲得CDE批準(zhǔn)在中國(guó)上市。2023年11月16日,艾貝格司亭α成功獲得FDA批準(zhǔn)在美國(guó)上市。
圖1. 文章在線(xiàn)發(fā)表于Supportive Care in Cancer雜志
研究背景
化療導(dǎo)致的中性粒細(xì)胞減少癥(Chemotherapy-induced neutropenia,CIN)和發(fā)熱性中性粒細(xì)胞減少癥(febrile neutropenia,F(xiàn)N)會(huì)增加患者的感染風(fēng)險(xiǎn),導(dǎo)致化療藥物的減量或給藥延遲,嚴(yán)重者甚至危及患者生命。
因此,預(yù)防CIN的發(fā)生是保證足劑量化療的重要方面。NCCN等指南建議對(duì)于FN高風(fēng)險(xiǎn)患者(>20%)和FN中風(fēng)險(xiǎn)(10%-20%)伴危險(xiǎn)因素的患者預(yù)防性給予重組人粒細(xì)胞集落刺激因子(rhG-CSF)。
艾貝格司亭α(Efbemalenograstim alfa,研發(fā)代號(hào)F-627)是一種新型的長(zhǎng)效雙分子G-CSF-Fc融合蛋白,其預(yù)防CIN的效力已在臨床前和II期臨床研究中得到初步證實(shí)。在II期研究中,艾貝格司亭α在降低嚴(yán)重(4級(jí))中性粒細(xì)胞減少癥的平均持續(xù)時(shí)間(DSN)方面,非劣效于培非格司亭和非格司亭。本研究(NCT02872103)是艾貝格司亭α第一個(gè)關(guān)鍵性III期研究,旨在評(píng)估艾貝格司亭α用于降低接受骨髓抑制性化療的乳腺癌患者FN風(fēng)險(xiǎn)的有效性和安全性。
研究設(shè)計(jì)
本研究為全球、多中心、隨機(jī)、雙盲、安慰劑對(duì)照的III期臨床研究,由加州大學(xué)洛杉磯分校醫(yī)學(xué)院(UCLA School of Medicine)的John Glaspy作為主要研究者,在全球16個(gè)中心進(jìn)行。接受4個(gè)周期TA方案(75 mg/m2紫杉醇/多西他賽+ 60 mg/m2多柔比星)的II-IV期乳腺癌患者,以2:1的比例(按國(guó)家/地區(qū)分層)隨機(jī)分配到艾貝格司亭α組或安慰劑組,在第一個(gè)周期化療給藥后約24小時(shí)皮下注射20 mg艾貝格司亭α或安慰劑,之后的化療周期所有的受試者均給予艾貝格司亭α。主要有效性終點(diǎn)為首個(gè)化療周期內(nèi)觀(guān)察到4級(jí)(重度)中性粒細(xì)胞減少癥(ANC<0.5×109/L)的持續(xù)時(shí)間。
研究結(jié)果
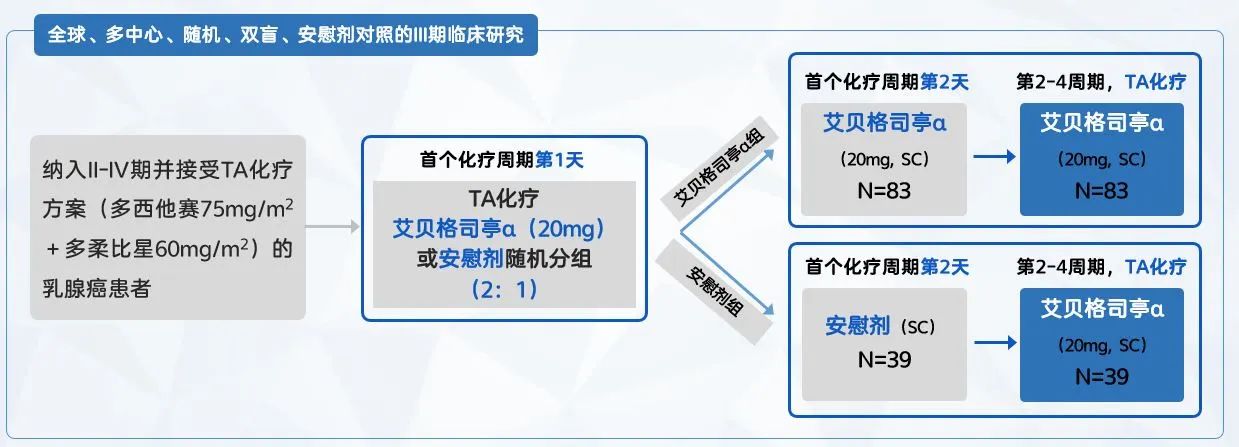
圖2. 試驗(yàn)設(shè)計(jì)
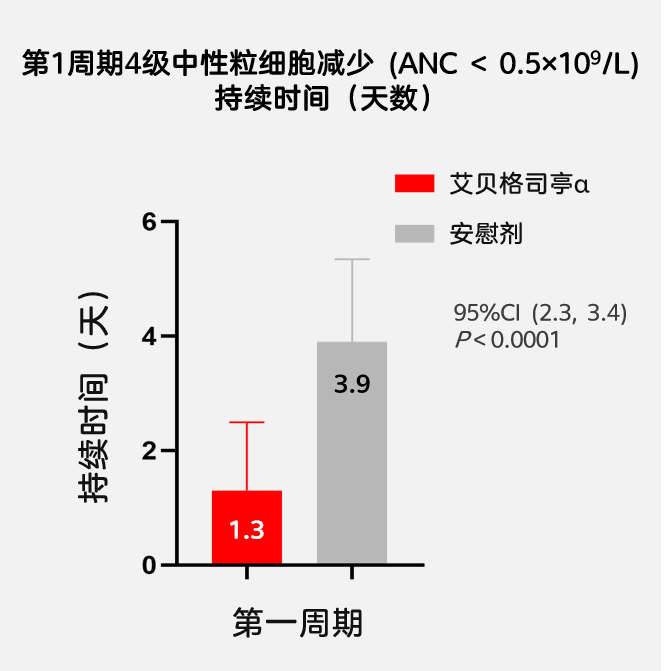
圖3. 第1周期嚴(yán)重中性粒細(xì)胞減少癥(ANC < 0.5×109/L)的持續(xù)時(shí)間(天數(shù))
表1. 第1周期次要有效性指標(biāo)分析
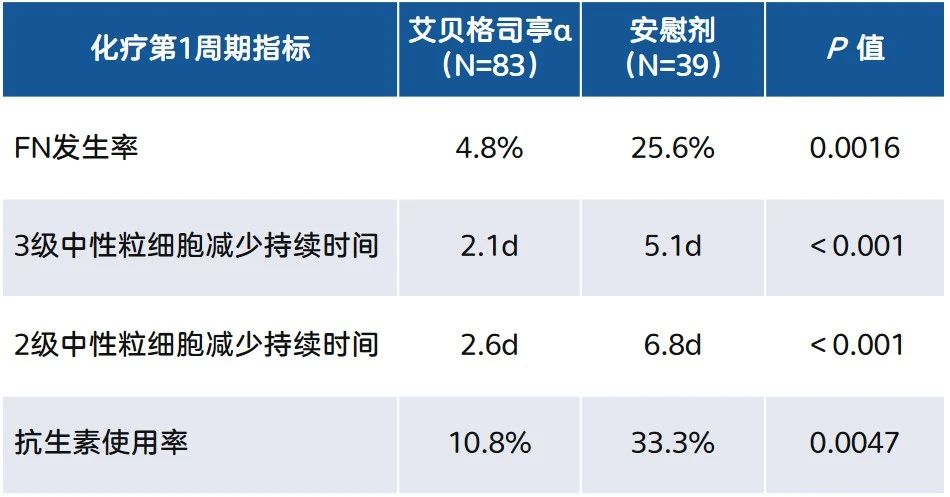
次要終點(diǎn)方面,艾貝格司亭α組和安慰劑組在第1周期的FN發(fā)生率分別為4.8%和25.6%,差異具有統(tǒng)計(jì)學(xué)意義。艾貝格司亭α組在第1周期的抗生素使用率為10.8%,遠(yuǎn)低于安慰劑組(33.3%)(表1)。此外,與安慰劑組相比,艾貝格司亭α組第1周期的3級(jí)和2級(jí)中性粒細(xì)胞減少的持續(xù)時(shí)間顯著縮短(表1)。
尤其值得注意的是,艾貝格司亭α組在第1周期的中性粒細(xì)胞計(jì)數(shù)(ANC)最低點(diǎn)及其恢復(fù)時(shí)間方面表現(xiàn)更佳。在第1周期中,艾貝格司亭α組和安慰劑組分別在第8天和第10天達(dá)到ANC最低點(diǎn),ANC最低點(diǎn)的平均中性粒細(xì)胞數(shù)分別為0.7×109/L和0.2×109/L,兩組的比率為3.4(95%CI:2.0, 5.6)(圖4)。而且,在艾貝格司亭α組受試者中觀(guān)察到更快的ANC恢復(fù),與安慰劑組從ANC最低點(diǎn)恢復(fù)至2×109/L需要4.1天相比,艾貝格司亭α組的恢復(fù)時(shí)間為2.1天,平均差異為 2.0 天(圖4)。
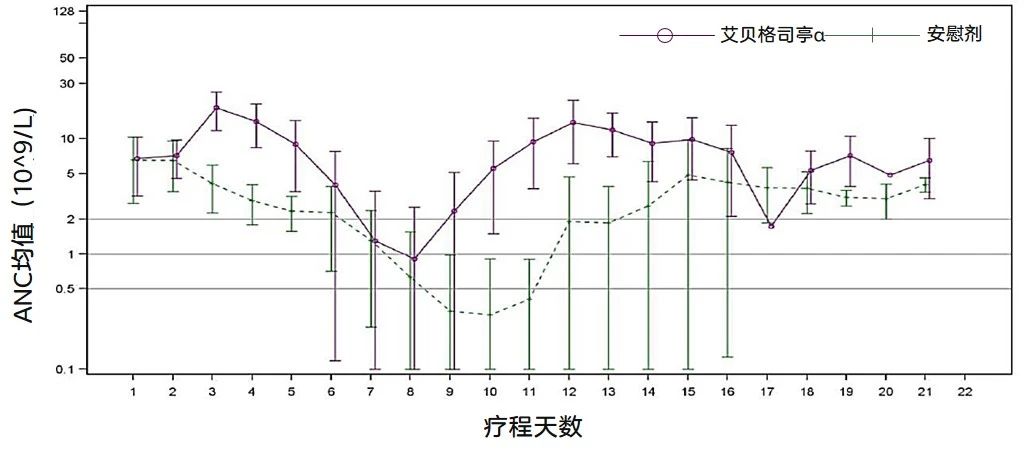
圖4. 第一周期的平均中性粒細(xì)胞計(jì)數(shù)
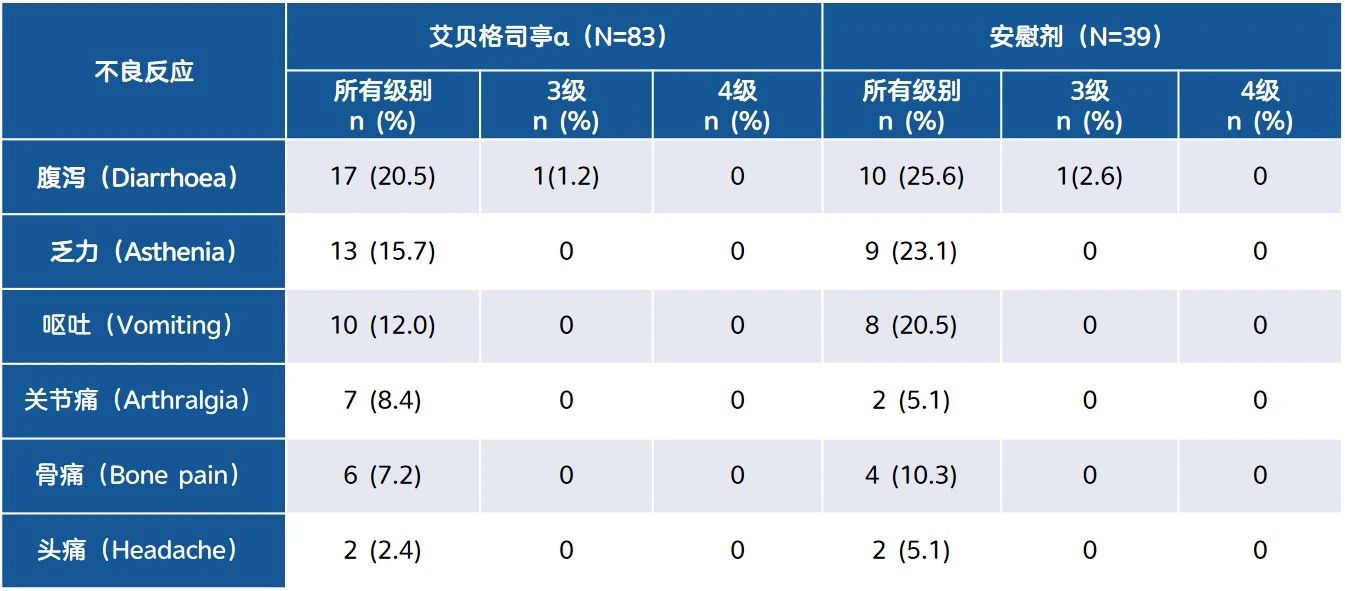
安全性方面,骨痛是與G-CSF相關(guān)的主要不良事件,在艾貝格司亭α組和安慰劑組中分別報(bào)告了7.2%和10.3%的受試者發(fā)生了骨痛。所有骨痛均為輕度至中度(表2)。除了來(lái)自于化療方案的不良事件(例如惡心、嘔吐、腹瀉、脫發(fā)、疲勞等),本研究未報(bào)告其他被認(rèn)為可能歸因于G-CSF及其衍生物的不良事件(如脾破裂、鐮狀細(xì)胞性貧血伴危象、急性呼吸窘迫綜合征等)。
表2. 第1周期主要不良反應(yīng)總結(jié)
結(jié)語(yǔ)
總體而言,該研究表明了艾貝格司亭α能夠顯著降低化療相關(guān)的發(fā)熱性中性粒細(xì)胞減少的發(fā)生率,縮短嚴(yán)重中性粒細(xì)胞減少的持續(xù)時(shí)間,其療效確切,安全性可耐受。作為新型的長(zhǎng)效G-CSF-Fc融合蛋白,艾貝格司亭α有望成為接受骨髓抑制性化療患者預(yù)防中性粒細(xì)胞減少癥的有效武器,為腫瘤患者完成足劑量、足療程化療保駕護(hù)航。
參考文獻(xiàn):
Glaspy J, Bondarenko I, Burdaeva O, et al. Efbemalenograstim alfa, an Fc fusion protein, long-acting granulocyte-colony stimulating factor for reducing the risk of febrile neutropenia following chemotherapy: results of a phase III trial[J]. Supportive Care in Cancer, (2024) 32:34. https://doi.org/10.1007/s00520-023-08176-6.