新聞中心
News Center
ASCO上再現輝煌!中國生物制藥“得福組合”頭對頭戰勝K藥
發布時間:2025-06-02

全球首個抗PD-L1單抗聯合多靶點抗血管TKI一線治療PD-L1陽性非小細胞肺癌的III期臨床研究結果揭曉!當地時間6月1日,中國生物制藥(1177.HK)以最新重磅摘要(LBA)形式披露CAMPASS研究數據,“得福組合”——貝莫蘇拜單抗(安得衛®)聯合安羅替尼(福可維®)頭對頭戰勝K藥,展示出國產創新藥的過硬實力。這是“得福組合”繼頭對頭戰勝替雷聯合化療用于一線鱗狀非小細胞肺癌(sq-NSCLC)后,在非小細胞肺癌治療領域再續傳奇,展示出“得福組合”極具潛力的臨床價值,以及國產創新藥對于提高稀缺藥物可及性的經濟價值和社會價值。

(韓寶惠教授在大會現場作報告)
接連戰勝K藥、替雷,“得福組合”首創性研究直面臨床困境
2022年全球癌癥數據統計顯示,肺癌在全球和中國的發病率及死亡率居所有惡性腫瘤的第一位,其中非小細胞肺癌(NSCLC)占全部肺癌的80%-85%[1]。長期以來,被譽為全球藥王的“K藥”——帕博利珠單抗單藥治療一直是PD-L1陽性晚期非小細胞肺癌患者的標準一線治療方案之一,但中位無進展生存期(PFS)僅為約6個月[2],患者亟需更優治療選擇。
安羅替尼是目前國內唯一批準的用于非小細胞肺癌三線及以上治療的多靶點抗血管TKI,可以同時兼顧腫瘤及其微環境,臨床應用中既可“獨當一面”,又為“良好搭檔”,能有效地改善免疫抑制的腫瘤微環境,增加腫瘤組織內免疫活性CD8+T細胞數量、減少免疫抑制FoxP3+Treg細胞浸潤,顯著提高CD8/FoxP3細胞比例。貝莫蘇拜單抗是一款創新人源化抗PD-L1單克隆抗體,與安羅替尼聯用,具有協同增效的作用。
目前,“得福組合”用于治療廣泛期小細胞肺癌、子宮內膜癌、腎細胞癌的適應癥已獲批上市,針對晚期sq-NSCLC患者的一線治療、Ⅲ期不可切除NSCLC患者的鞏固治療上市申請均已受理,另有多個適應癥研究正在進行中。本次ASCO大會還將以口頭報告形式公布“得福組合”頭對頭戰勝替雷利珠單抗聯合化療III期研究詳細數據。“得福組合”取得mPFS 10.12個月,疾病進展/死亡風險降低36%的顯著優效,將開創肺鱗癌一線治療新模式。
臨床價值凸顯,提升PD-L1高表達人群中位PFS超過6個月
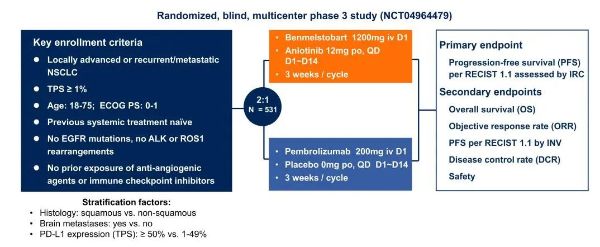
CAMPASS研究是一項隨機對照Ⅲ期臨床研究,共納入531例PD-L1表達陽性(定義為TPS≥1%)的局部晚期(IIIB/C期)或復發/轉移性非小細胞肺癌受試者。受試者以2∶1比例隨機分組,分別接受“得福組合”或帕博利珠單抗聯合安慰劑治療,主要終點為IRC根據RECIST 1.1評估的無進展生存期(PFS) 。
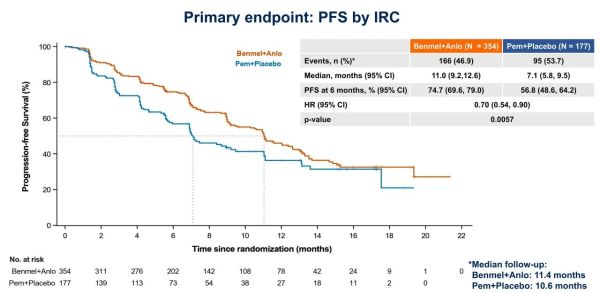
結果顯示[3]:
●本次公布的結果為主要終點PFS的最終分析數據,“得福組合”治療組和帕博利珠單抗治療組的中位隨訪時間分別為11.4月和10.6月,數據成熟穩健。
●在全人群中,“得福組合”中位PFS達到11.0個月,較帕博利珠單抗治療提升3.9個月,疾病進展或死亡風險降低30%(HR=0.70)。
●亞組分析顯示,幾乎所有亞組均可從“得福組合”方案中獲益。特別值得一提的是,對于TPS≥50%人群,“得福組合”較帕博利珠單抗治療,中位PFS提升6.1個月,疾病進展/死亡風險降低40%(HR=0.60)。結合臨床實踐中更傾向給TPS≥50%患者使用無化療方案,凸顯了本研究巨大的臨床價值。
●聯合治療經確認的腫瘤客觀緩解率(ORR)為57.3%(帕博利珠單抗治療組為39.5%),疾病控制率(DCR)為85.9%(帕博利珠單抗治療組為79.1%),均有顯著性提升。
此外,“得福組合”還展現出安全可控、耐受性好等特點。多靶點抗血管TKI聯合免疫治療,安全性一直是臨床關注的焦點,也是影響患者臨床獲益的“痛點”。本研究中,“得福組合”未提示新的安全性信號,治療相關不良事件導致任意藥物永久終止治療的發生率(7.1% vs. 8.0%)和死亡率(1.4% vs. 2.3%),“得福組合”均略低于帕博利珠單抗治療組,切實保障了患者獲益。

免疫檢查點抑制劑的出現,極大改善了驅動基因陰性非小細胞肺癌一線治療的患者預后。但學術界也一直在思考如何進一步提高一線免疫治療的療效。除了傳統的聯合化療,免疫治療聯合抗血管治療是迄今為止公認最有效的聯用增效策略。
安羅替尼是目前非小細胞肺癌三線治療的標準藥物,也是迄今唯一一個在后線Ⅲ期隨機對照研究中取得總生存期顯著獲益的小分子多靶點抗血管藥物。貝莫蘇拜單抗是一款新型抗PD-L1單抗,為免疫治療提供了新的有力武器。此前,在課題組開展的探索研究中,“得福組合”在NSCLC的后線治療中已經取得了非常好的表現。
此次公開的CAMPASS研究,進一步將 “得福組合” 推向 NSCLC一線治療,這不僅是課題組前期探索研究成果的重要延伸,更是迄今為止國際上首個抗 PD-L1單抗與多靶點小分子抗血管藥物組合用于 NSCLC 一線治療的Ⅲ期頭對頭研究,其設計具有開創性與前瞻性。
作為全球首個對比帕博利珠單抗治療取得陽性結果的抗PD-L1單抗聯合多靶點小分子抗血管藥物組合,這一聯用方案或將為PD-L1陽性的晚期非小細胞肺癌患者提供更優的一線治療選擇。

我們的研究證實,安羅替尼是唯一既能通過血管正常化消除腫瘤“物理保護屏障”,也能通過下調腫瘤血管內皮細胞PD-L1表達消除“生物保護屏障”、促進免疫細胞突入瘤灶的血管靶向治療“多面手”,最適合增效免疫治療。
本研究的一大亮點是其對PD-L1高表達(TPS≥50%)人群的療效,雖然目前對這部分人群已形成了“單免治療”共識,但由于帕博利珠單抗治療的PFS仍然相對有限,有些同道仍對“去化療”做法存疑。此次貝莫蘇拜單抗聯合安羅替尼將中位PFS提升了6.1個月,達到13.3個月,這一關鍵突破也無可辯駁地奠定了“得福組合”在此人群中的主導治療地位。
本研究的另一個特點是良好的安全和耐受性,研究中≥3級治療相關不良事件主要為多靶點抗血管藥物的常見不良反應且較好處理,治療相關嚴重不良事件發生率兩組比較接近。在最初進行研究方案設計時,我們就制定了詳細的安羅替尼劑量調整建議,可以在保障治療效果的同時有效提高治療耐受性。
這項研究的結果證實了“得福組合”能夠較K藥顯著改善PD-L1陽性晚期非小細胞肺癌患者的無進展生存期,期待這一治療組合盡快獲批,早日造福患者。

此次 “得福組合” 頭對頭戰勝 “藥王” K 藥,是國產創新藥里程碑式的突破。這不僅是一組臨床試驗數據的勝利,更是中國創新藥研發實力的有力證明。
從在多個適應癥上展現出巨大的治療潛力,到接連擊敗國際重磅藥物,“得福組合” 的臨床表現令人鼓舞。繼頭對頭戰勝替雷后,能夠頭對頭戰勝全球“藥王”K藥,更是標志著國產創新藥在癌癥治療方面已經站在國際的最前沿。
未來,中國生物制藥將持續深耕創新,加速推進 “得福組合” 等創新產品走向市場,讓中國原研藥惠及更多患者,助力中國醫藥創新從 “并跑者” 成為 “領跑者”!

參考文獻:
[1] Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA. Cancer J. Clin. 2024, 74(3): 229-263.
[2] Wu YL, Zhang L, Fan Y, et al. Randomized clinical trial of pembrolizumab vs chemotherapy for previously untreated Chinese patients with PD-L1-positive locally advanced or metastatic non-small-cell lung cancer: KEYNOTE-042 China Study. Int J Cancer. 2021, 148(9): 2313-2320.
[3] Han BH, et al. CAMPASS: Benmelstobart in combination with anlotinib vs pembrolizumab in the first-line treatment of PD-L1 positive, advanced non-small cell lung cancer (aNSCLC): A randomized, blind, multicenter phase 3 study. 2025 ASCO (LBA8502).
聲明:
1.新聞稿旨在促進醫藥信息的溝通和交流,僅供醫療衛生專業人士參閱,非廣告用途。
2.本公司不對任何藥品和/或適應癥作推薦。
3.本新聞稿中涉及的信息僅供參考,不能以任何方式取代專業的醫療指導,也不應被視為診療建議。若您想了解具體疾病診療信息,請遵從醫生或其他醫療衛生專業人士的意見或指導。
前瞻性聲明:
本新聞稿中包含若干前瞻性陳述,包括有關【貝莫蘇拜單抗、鹽酸安羅替尼】的臨床開發計劃、臨床獲益與優勢的預期、商業化展望、患者臨床獲益可能性,以及潛在商業機會等聲明。“預期”、“相信”、“繼續”、“可能”、“估計”、“期望”、“有望”、“打算”、“計劃”、“潛在”、“預測”、“預計”、“應該”、“將”、“擬”、“會”和類似表達旨在識別前瞻性陳述,但并非所有前瞻性陳述都包含這些識別詞。這些前瞻性陳述為公司基于當前所掌握的數據和信息所做的預測或期望,可能因受到政策、研發、市場及監管等不確定因素或風險的影響,而導致實際結果與前瞻性陳述有重大差異。請現有或潛在的投資者審慎考慮可能存在的風險,并不可完全依賴本新聞稿中的前瞻性陳述,該等陳述包含信息僅及于本新聞稿發布當日。除非法律要求,本公司無義務因新信息、未來事件或其他情況而對本新聞稿中任何前瞻性陳述進行更新或修改。